Les chaînes d’approvisionnement médical jouent un rôle essentiel dans la livraison des produits de santé essentiels et dans la disponibilité des médicaments et des fournitures médicales, en particulier dans les pays en développement. Bien que la Zambie se concentre sur le secteur des soins de santé primaires (SSP) et s’engage à améliorer l’efficacité du système de santé, il existe des défis opérationnels persistants tels que les retards dans l’approvisionnement, une visibilité incomplète du suivi et des capacités de stockage inadéquates. De nombreux défis subsistent. La plupart sont liés aux produits contrefaits observés à plusieurs étapes de la chaîne d’approvisionnement. Pour surmonter les difficultés, fin octobre 2021, l’Autorité zambienne de réglementation des médicaments (ZAMRA) a pris des mesures importantes pour mettre en place des systèmes de traçabilité pharmaceutique. La ZAMRA a publié un projet de directive sur l’identification et l’étiquetage des médicaments et des substances apparentées et sur le partage des données de base pour recueillir les commentaires et les réactions du public. Le principal objectif de la Zambia Medicines Regulatory Authority est de veiller à ce que tous les médicaments et substances apparentées mis à la disposition de la population zambienne répondent systématiquement aux normes de qualité, de sécurité et d’efficacité établies. La ZAMRA espère créer des efficiences dans les chaînes d’approvisionnement de la santé publique et privée grâce à l’identification standardisée, à la saisie automatisée des données et à la réduction des coûts de mise en conformité. Plus précisément, les normes mondiales d’étiquetage et d’emballage visent à
Exigences en matière d’étiquetage et d’emballage des produits –
Tous les emballages tertiaires et secondaires doivent être étiquetés conformément aux exigences spécifiées en matière de code-barres, encodés et imprimés sous une forme lisible par l’homme. L’identification et l’étiquetage du niveau d’emballage primaire sont obligatoires si l’article est dans un emballage sans carton, c’est-à-dire sans emballage secondaire. Tous les symboles des codes-barres doivent être de qualité d’impression « Grade C » (1,5 ou plus).
Exigences en matière de codes-barres pour les emballages tertiaires –
Le code-barres de l’unité logistique est présenté de manière concaténée.
| Attributs des données | Valeurs | Identifiant de l’application | Informations complémentaires |
|---|---|---|---|
| SSCC | Code du conteneur d’expédition en série pour identifier l’unité logistique | 00 | Conformément à la spécification générale de GS1, un code sériel de conteneur d’expédition peut être réutilisé après une période d’un an. |
Symbole – GS1 128 :

Exigences en matière de codes-barres pour les emballages secondaires –
L’emballage secondaire est un niveau d’emballage qui peut contenir un ou plusieurs emballages primaires ou un groupe d’emballages primaires contenant un seul article.
| Attributs des données | Valeurs | Identifiant de l’application | Informations complémentaires |
|---|---|---|---|
| GTIN 14 | Les GTIN sont attribués par le propriétaire de la marque (MAH) de l’article commercial et sont utilisés pour identifier les articles commerciaux. | 01 | http://www.gs1.org/gtin https://www.gs1.org/1/gtinrules/en/healthcare |
| Date d’expiration | Le champ de données contient une date d’expiration (AAAA/MM/JJ). | 17 | Année : les dizaines et unités de l’année (par exemple, 2003 = 03), obligatoirement Mois : le numéro du mois (par exemple, janvier = 01), obligatoirement Jour : le numéro du jour du mois concerné (par exemple, deuxième jour = 02), facultatif |
| Numéro de lot | Le champ de données contient un numéro de lot. Le champ du numéro de lot est alphanumérique (jusqu’à 20 caractères). | 10 | |
| Numéro de série | Combiné à un GTIN, le numéro de série identifie de manière unique un article individuel. Le fabricant détermine le numéro de série. (Alphanumérique jusqu’à 20 caractères) | 21 |
Symbole – Matrice de données 2D GS1 :
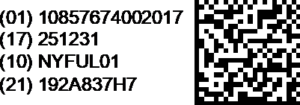
Exigences en matière de codes-barres pour l’emballage primaire –
S’il est mis en œuvre, l’identifiant unique de l’emballage primaire doit comprendre une matrice de données GS1 codée avec les informations suivantes et imprimée à côté du support de données sous une forme lisible par l’homme.
| Attributs des données | Valeurs | Identifiant de l’application | Informations complémentaires |
|---|---|---|---|
| GTIN 14 | Les GTIN sont attribués par le propriétaire de la marque (MAH) de l’article commercial et sont utilisés pour identifier les articles commerciaux. | 01 | http://www.gs1.org/gtin https://www.gs1.org/1/gtinrules/en/healthcare |
| Date d’expiration | Le champ de données contient une date d’expiration (AAAA/MM/JJ). | 17 | Année : les dizaines et unités de l’année (par exemple, 2003 = 03), obligatoirement Mois : le numéro du mois (par exemple, janvier = 01), obligatoirement Jour : le numéro du jour du mois concerné (par exemple, deuxième jour = 02), facultatif |
| Numéro de lot | Le champ de données contient un numéro de lot. Le champ du numéro de lot est alphanumérique (jusqu’à 20 caractères). | 10 | |
| Numéro de série | Combiné à un GTIN, le numéro de série identifie de manière unique un article individuel. Le fabricant détermine le numéro de série. (Alphanumérique jusqu’à 20 caractères) | 21 |
Symbole – Matrice de données 2D GS1 :
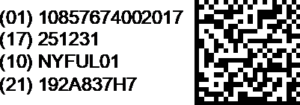
Jekson sur la régulation de la Zambie –
Reetrak (L3 ) est une solution de suivi et de traçabilité conçue pour lutter contre la contrefaçon et la distribution non autorisée. Reetrak échange des informations de manière transparente entre les différents systèmes informatiques et équipements impliqués dans la sérialisation et l’agrégation. Reetrak est essentiel pour les activités au niveau du site et est donc responsable de la communication des données du niveau de l’usine au niveau de l’entreprise. Les technologies de pointe pour la sérialisation et l’agrégation, les solutions d’inspection par vision et la vérification des codes à barres sont essentielles pour lutter contre la contrefaçon et assurer la conformité réglementaire de la Zambie. Reetrak de Jekson peut aider les propriétaires de marques/fabricants à se conformer aux réglementations du monde entier, en soutenant principalement les normes et les meilleures pratiques de l’industrie. Au fur et à mesure que la ZAMRA progresse dans ses plans de traçabilité, on suppose que, comme d’autres pays africains, la ZAMRA disposera de sa propre structure de rapport où les propriétaires de marques/fabricants communiqueront les détails de leur production.
ReeSource (L4) de Jekson est une solution SaaS complète qui aide les acteurs de la chaîne d’approvisionnement à se conformer à la plupart des réglementations pharmaceutiques mondiales.
Principales caractéristiques de ReeSource dans le cadre des opérations commerciales
- Sérialisation des produits et dépôt des numéros de série (conforme aux normes GS1)
- Référentiel EPCIS et protocole de communication EPCIS (conforme aux standards GS1)
- Visibilité de la chaîne d’approvisionnement de bout en bout
- Solution d’entreposage basée sur l’informatique en nuage
- Authenticité du produit (visibilité pour le consommateur final)
- Programmes conviviaux
La ZAMRA devrait finaliser et publier les directives pharmaceutiques au début de l’année 2022. Une fois publiées, la Zambie sera le deuxième pays d’Afrique subsaharienne, le premier étant l’Éthiopie, à avoir mis en place les directives réglementaires nécessaires à la traçabilité des produits pharmaceutiques à l’aide des normes GS1. En outre, ce travail est soutenu par le leadership du ministère de la santé. Cette directive s’appliquera à tous les médicaments destinés au marché zambien. Pour en savoir plus sur la manière dont Jekson Solutions se conforme à la réglementation zambienne, contactez-nous à l’adresse marketing@jeksonvision.com.







